Hoy vamos a comentar las características de una de las técnicas más potentes que existen en el ámbito del análisis químico hoy en día, la espectrometría de masas. Aunque realmente es una técnica completa e independiente puede ser acoplada a otras técnicas para complementar o añadir ciertas ventajas. Hoy, en primer lugar, empezaremos viendo la espectrometría de masas como detector para cromatografía (ya que así se llama el post) pero al final comentaremos muchas de las posibilidades que presenta como técnica en general. Empezamos...
¿Qué es la espectrometría de masas?
La espectrometría de masas (MS) es una técnica que se basa en separar iones en fase gaseosa dependiendo de su relación masa/carga, de manera que si somos capaces de darle a una molécula o átomo una sóla carga somos capaces de medir su masa molecular. Con ello, no sólo somos capaces de detectarlo, si no que además podemos seleccionar medir únicamente la molécula que nos interesa o uno de sus fragmentos.
Además de esta ventaja con respecto a otros detectores, los límites de detección con esta técnica son unos de los mejores (en muchos casos con mucha diferencia), pudiendo llegar a detectar partes por trillón (americano) de muchas sustancias (1 entre 1.000.000.000.000). En casos extremos, como en el detector Orbitrap, según los desarrolladores, son capaces de detectar una sóla molécula siempre que tenga al menos 5 cargas.
En los espectrómetros de masas hay que diferenciar 3 partes bien diferenciadas:
- La fuente de iones: Es la parte del sistema encargada de convertir las moléculas (o átomos) en iones. Esta parte del sistema es muy importante, ya que dependiendo de la fortaleza de la ionización se obtendrán más fragmentos o menos, llegando en los casos más extremos a separar la molécula en iones o, en los casos más débiles, a obtener agregados de moléculas con muy pocas cargas. Por tanto, la interpretación del espectro de masas dependerá de la elección de la fuente de ionización. También hay que tener en cuenta que estas fuentes de ionización sirven como interfases entre el cromatógrafo y el analizador, habiendo incompatibilidades en algunos casos que comentaremos más adelante.
- El analizador: Es la parte del sistema que se encarga de separar y/o filtrar los iones. Se podría decir que es el corazón del analizador de masas ya que dependiendo del tipo de analizador obtendremos mayor o menor resolución entre los picos de las masas. Es la parte más cara y más grande del sistema, necesita muy alto vacío y suele ser la parte más grande y sensible del equipo, dependiendo el coste del sistema, principalmente, del analizador elegido.
- El sistema de detección: Es la última parte del equipo, la responsable de transducir los impactos de los iones en una señal eléctrica medible por un ordenador. Habitualmente se trata de algún tipo de multiplicador de electrones, siendo los más habituales la copa de Faraday o el detector ion-to-photon, dependiendo principalmente del nivel de concentración empleado. Es común que un equipo funcione con varios detectores a la vez. Existen analizadores, como en el caso del FT-ICR o el Orbitrap que ellos mismos sirven como sus propios detectores a partir de la corriente eléctrica inducida en su superficie.
Por tanto, vamos a ver cada una de estas partes aplicadas al acoplamiento con sistemas cromatográficos, principalmente de líquidos y de gases. Además veremos las posibilidades que ofrece cada combinación fuente+analizador para cada tipo de cromatografía. Empezaremos echando un vistazo a las fuentes de iones, clasificadas de más fuertes a más débiles; a continuación los analizadores de los más sencillos a los más complicados; la espectrometría de masas en tándem y, por último, algunas aplicaciones.
Fuentes de ionización
Plasma acoplado inductivamente (ICP)
El plasma acoplado inductivamente (Inductively Coupled Plasma, ICP) es la técnica de ionización más dura, más fuerte. Es tan fuerte que separa todos los átomos presentes y los ioniza en unas pocas décimas de segundo. Esto es posible a la antorcha de plasma de Argon a unos 8-10.000 K, aproximadamente la temperatura de la superficie del Sol. Esta técnica está especialmente indicada para el análisis de metales a niveles de traza y ultratraza en matrices acuosas.
 |
| Etapas en ICP-MS (Laboratorio ICP-MS-SIdI-UAM) |
Esta técnica se puede utilizar sin acoplar a ninguna otra técnica, pero su acoplamiento a LC o electroforesis capilar proporciona la capacidad de separar las especies que contienen los mismos átomos. Tengo mis dudas con respecto al acoplamiento con GC, aunque compuestos metálicos estables en fase gas no hay demasiados.
Como he comentado anteriormente, esta técnica está especialmente diseñada para el análisis de metales, ya que hay algunos átomos que no es capaz de ionizar. Estos son H, He, C, N, O, F y Ne. El análisis de otros átomos, como son Cl, S, I, Br y gases nobles en general, presenta otras dificultades, tales como solapamientos de masas (distintos isótopos de diferentes metales con el mismo peso atómico) o el solapamiento de aductos con la misma masa que el isótopo de interés, por ejemplo, la medida de Se en matrices marinas crea un aducto Ar-Cl (m/z 75) de la misma masa que el isótopo principal del Se.
Para evitar estos solapamientos se han desarrollado diferentes aproximaciones para eliminar estas interferencias, desde el KED (Kinetic Energy Discrimination) que hace colisionar los iones con He , eliminando los iones con mayor radio (normalmente los aductos) o la DRC (Dinamic Reaction Cell) que hace reaccionar los aductos con un gas, habitualmente metano o amoníaco, para romperlos y eliminar la interferencia.
Otra posibilidad es emplear un analizador de alta resolución, capaz de separar milésimas de unidades atómicas y así poder diferenciar, por ejemplo, el S del O2 o el 40Ar, generador del plasma.
El analizador típico es el cuadrupolo, debido a que la resolución necesaria suele ser de 1 m/z, aunque se pueden utilizar analizadores con mayor poder de resolución.
Si quieres más información, en la página del Dr. Ramón Fernández (RTL del laboratorio TXRF-SIdI-UAM) explica todo con mucho más detalle.
Impacto electrónico (EI)
El impacto electrónico es la primera técnica que existió de ionización para MS, siendo una técnica dura, que produce buenas fragmentaciones y que es la que se enseña principalmente en todas las asignaturas de determinación estructural. Hay que tener en cuenta que esta técnica es únicamente acoplable a GC.
 |
| Ionización por impacto electrónico Thilini ukwaththage (Own work), via Wikimedia Commons |
Esta técnica se basa en hacer pasar una corriente de gas a través de una cortina de electrones. Cuando un electrón impacta en una molécula, por repulsión electrostática, es capaz de arrancarle un electrón. Esta molécula deficiente de un electrón (catión radical) es capaz de reaccionar consigo misma fragmentándose. Las reacciones que se llevan a cabo dependen de la estructura de la molécula en cuestión, sus grupos funcionales, etc.
| Espectro de masas por impacto electrónico del tolueno |
Ionización química (CI, APCI)
La ionización química (Chemical Ionization, CI) trata de generar iones a partir de especies inestables que pueden sustraer, añadir o formar aductos cargados con las moléculas de un gas. Esta forma de ionización es más blanda y está basada en EI, ya que los iones primarios (de metano o amoníaco) se generan así. Para que los iones no colisionen con las moléculas del aire, la cámara de reacción se encuentra a vacío (aprox. 1 Torr), aunque actualmente existen equipos de APCI (Atmospheric Pressure Chemical Ionization) que trabajan a presión atmosférica con resultados muy buenos para HPLC y GC.
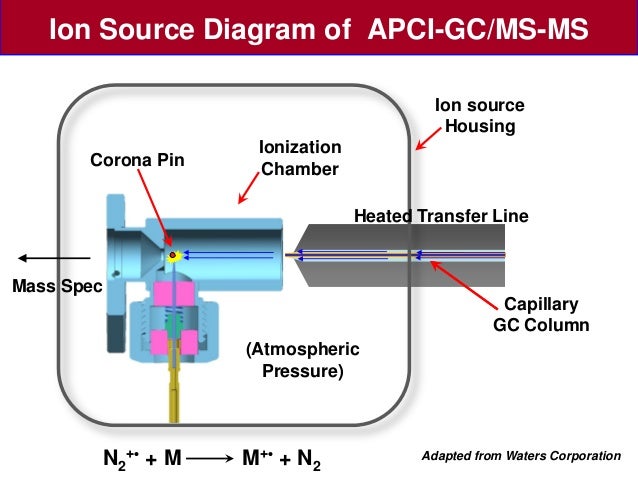 |
| Esquema APCI https://www.slideshare.net/WatersChemical/apci-and-appigcmsms-for-characterization-of-the-macondo-wellhead-crude-oil-and-the-oil-spill |
Electrospray (ESI)
La fuente de ionización por electrospray (ElectroSpray Ionization, ESI) es una de las fuentes más utilizadas en LC para el análisis de moléculas grandes, especialmente ADN y proteínas. Se basa en un capilar metálico cargado por el que fluye de manera muy lenta un líquido. Debido a la diferencia de potencial entre el capilar y un electrodo, normalmente uno de los conos, se produce un cono de líquido que, eventualmente, es capaz de arrojar diminutas gotitas hacia el electrodo. Estas gotas, en su viaje por el aire, sufren la evaporación del disolvente, haciéndose cada vez más pequeñas hasta que la repulsión electrostática de las cargas que contiene hace que la gota estalle.
| Ionización por electrospray https://www.researchgate.net/figure/Schematic-representation-of-the-electrospray-ionization-process-Adopted-from-33_fig5_307606559 |
Una vez que la gota estalla, los iones en fase gas son introducidos en el analizador para su separación y posterior medida. Tras la aparición de los sistemas de UHPLC y UPLC que emplean columnas capilares o semi-capilares, se desarrolló una interfase capaz de trabajar con esos caudales tan bajos, dando lugar al nanoelectrospray, capaz de trabajar, incluso, con volúmenes estáticos.
Analizadores
Dentro de los analizadores hay que tener en cuenta varios factores. Dependiendo del modo de medida se clasifica en TIC (Total Ion Current) en el que el analizador únicamente sirve para enfocar los iones en el detector, SCAN (modo barrido) en el que el analizador modifica sus parámetros de enfoque para "barrer" un intervalo específico de masas o en modo SIM (Single Ion Monitoring) en el que se monitorizan una o unas pocas m/z, obviando el resto del espectro de masas con intención de aumentar la sensibilidad.
De igual manera, otro factor importante en muchos casos es el poder de resolución, no confundir con la resolución de la separación cromatográfica, no vayamos a tener un disgusto. Esta resolución es el cociente de la masa a medir entre la anchura a media altura del pico de masas obtenido. Lo vemos mejor con esta imagen:
 |
| Poder de resolución http://fiehnlab.ucdavis.edu/projects/seven-golden-rules/mass-resolution |
Cuadrupolo (Q)
El analizador cuadrupolar (Quadrupole, Q) es el analizador más básico de todos y el que tiene menos resolución. Habitualmente se suele emplear para separar iones que no necesitan demasiada resolución. En los mejores casos se logran poderes de resolución de 1000, es decir, en masa 1000 Da tener una anchura de 1 Da, lo que es tener un poder de resolución bastante bajo.
Aún así, el analizador cuadrupolar es el más ampliamente utilizado de todos debido, principalmente, a su bajo coste, su nulo mantenimiento y su facilidad de modificación de parámetros. Consta de cuatro varillas (o polos) colocados paralelos y enfrentados dos a dos (en caso de ser 6 se llamaría hexapolo y, si son 8, octapolo). Estas varillas idealmente deberían tener forma hiperbólica pero, por facilidad de manufactura, muchas veces tienen forma de cilindro.
 |
| Analizador cuadrupolar http://www.tissuegroup.chem.vt.edu/chem-ed/ms/quadrupo.html |
A dos de las varillas se le aplica una diferencia de potencial eléctrico constante mientras que a las otras se les aplica una diferencia de potencial variable, haciendo que de todos los iones que viajan por su interior únicamente aquellos con una determinada m/z sean resonantes en el campo eléctrico creado y sean capaces de atravesar las varillas sin colisionar con ellas (descargándose) o salir despedidos entre las varillas.
Sector magnético
Fue el primer tipo de analizador de masas desarrollado y, actualmente, ha resurgido como un analizador de masas de alta resolución debido a la mejora de la electrónica y del control de campos eléctricos. Este analizador consta de dos placas metálicas curvas a las que se le aplica un distinto potencial eléctrico, de manera que son capaces de desviar los iones de manera que únicamente las atraviesen una m/z determinada.
 |
| Analizador de sector magnético http://orgchemguide.blogspot.com.es/2011/04/magnetic-deflection-or-sector-mass.html |
Debido a la "simpleza" de este detector su poder de resolución también es limitado, por lo que es habitual colocar dos sectores en tándem, como veremos más adelante.
Tiempo de vuelo (TOF)
Los analizadores de tiempo de vuelo (Time Of Flight, TOF) también fueron de los primeros en desarrollarse. Su funcionamiento se basa en la primera ley de Newton:
F = m · a
Estos analizadores almacenan durante pequeños instantes de tiempo los iones que le llegan para, a continuación, dispararlos a lo largo de un tubo a vacío. Debido a que la fuerza aplicada a todos los iones es la misma, aquellos con menos masa adquirirán mayor aceleración que aquellos más pesados, difiriendo en su llegada al final del tubo.
 |
| Analizador TOF https://www.shimadzu.com/an/lcms/support/intro/lib/lctalk/61/61intro.html |
Como en el caso del sector magnético, sufrió un renacimiento debido a la mejora de la electrónica, especialmente en la mejora para medir tiempos más pequeños, lo que permite mejorar el poder de resolución de estos equipos. Además, la introducción del reflectrón hizo que mejorase mucho el poder de resolución de estos equipos. El reflectrón es un dispositivo que se coloca al final del tubo y hace que los iones reboten, duplicando el camino recorrido por los iones, haciendo mayores las diferencias entre los pequeños y los grandes, aumentando enormemente el poder de resolución.
Trampa iónica (IT)
La trampa iónica (Ion trap, IT) consiste en un electrodo de anillo intercalado entre dos electrodos que hacen de tapa. Al igual que un sistema cuadripolar, la superficie interna de los electrodos es hiperboloidal, que se puede pensar como la entrada y salida de un cuadrupolo conectado en forma de anillo. Allí, debido al potencial aplicado los iones quedan atrapados dando vueltas dentro del anillo.
 |
| Analizador de trampa de iones https://www.shimadzu.com/an/lcms/support/intro/lib/lctalk/61/61intro.html |
Con la variación del potencial del anillo, los iones más ligeros con expulsados por fuerza centrífuga del anillo, creando una variación en la corriente inducida en las tapas del anillo, con lo que se puede obtener la cantidad de iones que estaban dando vueltas. Para vaciar el anillo, se aplica un potencial para expulsar todos los iones o se hace que choquen contra la superficie del anillo, descargándose.
Ciclotrón de resonancia iónica (FT-ICR)
Estos analizadores son muy poco comunes por ser muy grandes y muy caros (rondan casi el millón de euros) pero son los que tienen un poder de resolución mayor (superior a un millón, es decir, pueden sacar 5 o 6 decimales a la masa de un ión).
 |
| Fotografía de un ICR-MS http://chemistry.rutgers.edu/grad/msfacility |
Este analizador es un acelerador de partículas (ciclotrón), que trabaja con campos magnéticos muy potentes, que aceleran enormemente los iones. Estos iones acaban teniendo órbitas circulares estacionarias resonantes, como los electrones en el átomo. Mediante la aplicación de un pulso en la superficie exterior del equipo se produce una desviación de los iones de su órbita, que induce una corriente eléctrica en las tapas del acelerador. Esta corriente es una onda evanescente que, mediante una transformada de Fourier (Fourier Transform, FT) se convierte desde el dominio del tiempo al dominio de las masas.
 |
| Funcionamiento ICR-MS http://www.tissuegroup.chem.vt.edu/chem-ed/ms/ftms.html |
Es por esta razón, principalmente, por la que el analizador ICR es comúnmente conocido como FT-MS. También hay que tener en cuenta que este analizador es su propio detector, no necesitando ninguno de los detectores comentados al principio, haciendo que también sea más sensible.
Orbitrap
El Orbitrap es un analizador-detector de masas similar al ICR pero de un tamaño mucho menor desarrollado por Thermo Scientific en el año 2005 y mejorado en el año 2011. Se basa en dos bloques metálicos con forma de huso entre los que se aplica una diferencia de potencial. Entre ellos, se disparan los iones de manera excéntrica, haciendo que oscilen con una frecuencia diferente dependiendo de su masa.
Ya que según el dicho, más vale una imagen que mil palabras, en este caso dejo un video para que veas cómo funciona este Orbitrap. Lo que aparece antes del Orbitrap (C-Trap + Orbitrap) simplemente son filtros iónicos que redirigen los iones y eliminan las moléculas neutras que hayan podido pasar por el vacío.
 |
| Tamaño Orbitrap (arriba, 2005; abajo 2011) |
Movilidad iónica (IM)
El analizador de mobilidad iónica (IM) se basa en hacer avanzar los iones por un pequeño tubo con un gas en contra, haciendo que se separen de acuerdo a su m/z, debido a su dificultad para avanzar pero también con respecto a su radio aerodinámico, lo que proporciona una dimensión adicional a la separación cromatográfica. Estos detectores, frente a sus compañeros, no necesita vacío y puede funcionar a presión ambiente, lo que hace que, combinado con la ionización APCI, sea una potencial herramienta en el futuro para el trabajo de campo con un MS portátil.
Lamentablemente, este es el analizador que menos conozco y la información en internet es realmente escasa por lo que si alguien necesita más información no dude en pedirla o proponerlo como tema para un próximo post y así aprenderemos todos
 |
| Analizador de movilidad iónica https://www.vanderbilt.edu/viibre/structural-mass-spec.php |
Espectrometría de masas en tándem (MS/MS, MSn)
También existe la posibilidad de realizar una fragmentación, escoger uno de los iones resultantes y volverlo a fragmentar. A esto se le denomina espectrometría de masas en tándem (MS/MS). El más habitual es el triple cuadrupolo (QQQ) o el cuadrupolo-TOF (Q-TOF) en el que los primeros cuadrupolos actúan para separar los iones de la primera fragmentación, un segundo cuadrupolo con algún gas dentro (habitualmente helio) fragmenta los iones y el último analizador (Q o TOF) separa los iones de esa última fragmentación.
Hay analizadores que dentro de sí mismo pueden llevar a cabo diferentes fragmentaciones, como es el caso de las trampas iónicas, que pueden separar y fragmentar varias veces, denominándose MSn, donde n es el número de ciclos fragmentación-separación llevados a cabo.
Aplicaciones
Además de las aplicaciones obvias de estos analizadores debido a su sensibilidad y altas posibilidades dentro del análisis químico, me gustaría destacar dos aplicaciones muy concretas en las que el análisis por cromatografía-MS ha ayudado en gran medida:
Relación isotópica
La determinación de la relación isotópica es un campo bastante desconocido pero que ha ayudado a comprender bastante bien el mundo en el que vivimos y en el que unos nos comemos a los otros. Debido a las diferencias en los distintos isótopos de carbono (12 y 13) y nitrógeno (14 y 15) somos capaces de saber nuestra posición en la cadena trófica y qué animal se come a cual, ayudando a desvelar fraudes como en el caso del jamón de bellota, cuyos valores de estos isótopos es diferente a los alimentados con pienso.
Además, también se usa para conocer la distribución de ciertos metales de la dieta o de la alimentación de las plantas. Se realiza alimentando al ser objeto de estudio con una dieta rica en un isótopo poco común y viendo dónde se localiza.
Por último, pero no menos importante, esta aplicación tuvo cierta relevancia mediática cuando en el año 2006, al ciclista Floyd Landis se le retiró el Tour de Francia que había ganado por dopaje con testosterona, una hormona. Él se defendió diciendo que esa testosterona la había producido su propio cuerpo, pero los análisis por relación isotópica determinaron que su relación isotópica era diferente a la encontrada en la testosterona del análisis, por lo que era considerado dopaje. El título del Tour cayó entonces en Oscar Pereiro, segundo clasificado.
Proteómica
En este campo la introducción de la espectrometría de masas ha supuesto un gran avance. Además de poder obtener la masa molecular de proteínas enormes hemos sido capaces de secuenciarlas sin necesidad de recurrir a enzimas que las cortasen en pequeños fragmentos y luego montarlos como un rompecabezas. En este caso, la espectrometría de masas es capaz de romper selectivamente en los enlaces peptídicos, obteniendo diferentes fragmentos desde los dos extremos, siendo capaces a mano como mediante software informático secuenciar en un día una proteína que antiguamente habría llevado meses secuenciar.
Por hoy es suficiente, si has llegado hasta aquí del tirón te mereces un premio. Espero que hayas aprendido algo de este mundo tan pequeño como es la espectrometría de masas. Eso sí, recuerda que estas son sólo las posibilidades que ofrece al acoplamiento con cromatografía. Si tienes interés de las técnicas sin acoplar (que básicamente difieren en las técnicas de ionización) puedes sugerirlo aquí o en la página de Facebook, ya que puede que no seas la única persona interesada en ello. Además, la MS ofrece otro mundo de posibilidades aún muy poco conocidas con la MSI (Mass Spectrometry Imaging) imágen por espectrometría de masas, de la que espero hablar en algún post próximo pero de la que puedes buscar información.
Nos vemos la semana que viene!!
Cuídate!!

No hay comentarios:
Publicar un comentario